
- 絶対に覚えておくべき必須アミノ酸\(8\)種類
- \(\alpha-\)アミノ酸をマスターする上での基礎となる双性イオン
- 溶液の\(\rm{pH}\)によるアミノ酸の変化
を特にポイントとしています.また,受験勉強に役立つアミノ酸一覧表も作成しましたので,ぜひ活用してくださいね!それでは今日も頑張っていきましょう!
\(\alpha-\)アミノ酸ってどんなの?
自然界に存在には,約\(20\)種類の\(\alpha-\)アミノ酸が存在します.その中で,動物の体内で合成できず,外部から摂取しなければならない\(\alpha-\)アミノ酸のことを必須アミノ酸といいます.
ヒト(人間)では,\(8\)種類です.
必須アミノ酸は以下の\(8\)種類です.
イソロイシン・スレオニン・フェニルアラニン・メチオニン・バリン・トリプトファン・ロイシン・リジン
この覚え方としては,それぞれの物質の頭文字をとって,「イスふめばとろり」と私は覚えています!笑
この\(8\)種類という数字と,できればその名称も覚えてくださいね!
\(\alpha-\)アミノ酸の基本的な考え方を解説していきます.
まず\(\alpha-\)アミノ酸の基本はアラニンで,下の図の中の四角の部分にいろんなものが挿入されて,それぞれの特徴が出てきます.できれば,構造や特徴,分子量などを覚えて欲しいです!
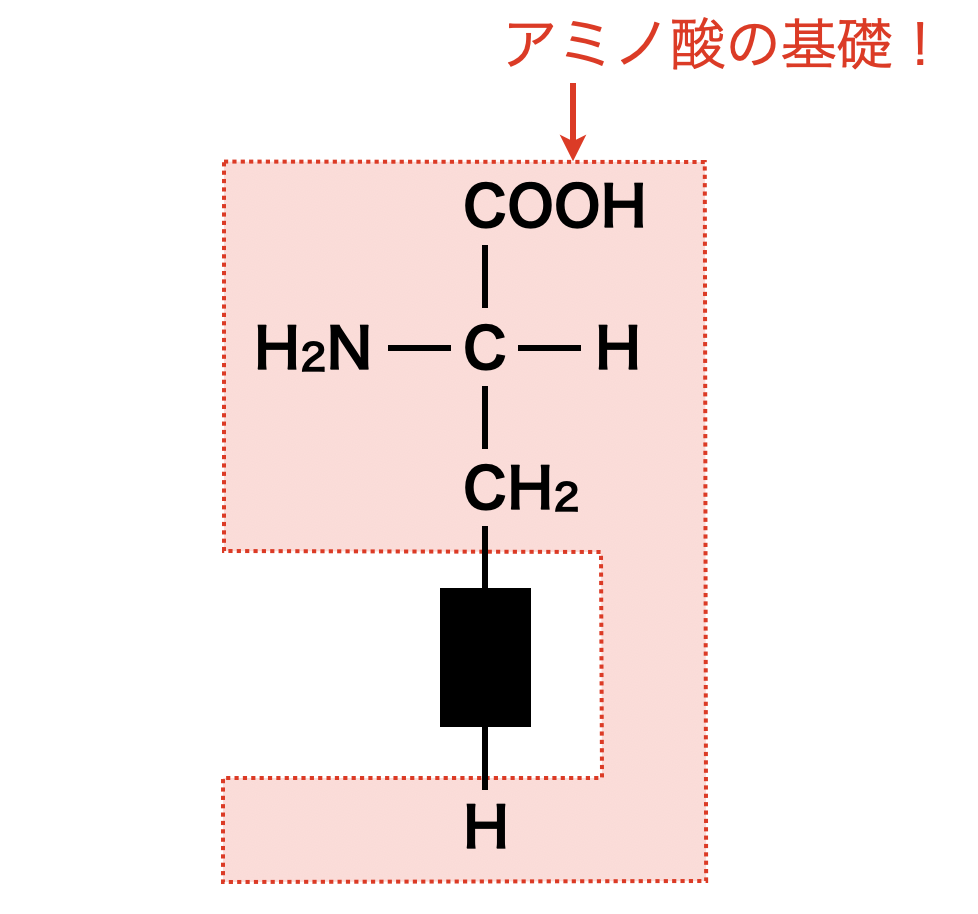
\(\alpha-\)アミノ酸には,側鎖の部分によって中性アミノ酸・酸性アミノ酸・塩基性アミノ酸の\(3\)種類があります.
- 中性アミノ酸:アミノ基×\(1\),カルボキシ基×\(1\)
- 酸性アミノ酸:アミノ基×\(1\),カルボキシ基×\(2\)
- 塩基性アミノ酸:アミノ基×\(2\),カルボキシ基×\(1\)
以上が基本の構造となります.細かい構造については下の\(\rm{PDF}\)に\(\alpha-\)アミノ酸の一覧をまとめているので,ぜひダウンロードして活用してくださいね!
↓↓↓
必須アミノ酸一覧表
\(\alpha-\)アミノ酸の反応
エステル化・アミド化・アセチル化
\(\alpha-\)アミノ酸は,アミノ基(\(\rm{-NH_2}\))が無水酢酸との反応でアセチル化します.
これはカルボキシ基のすきまにアミノ基の非共有電子対がそのすきまをうめる反応であるため,私は「すきま」「うめます」反応と呼んでいます.いつもの反応ですね!
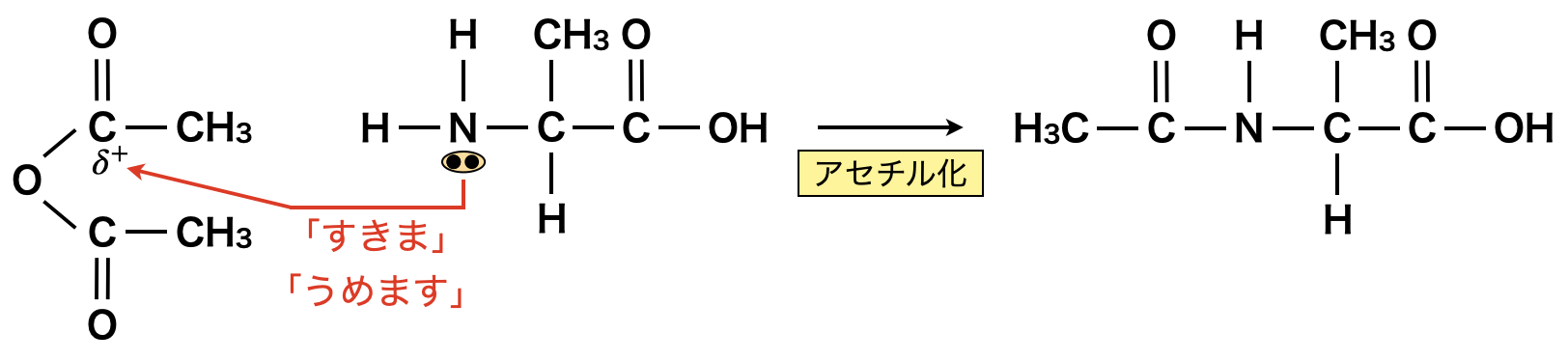
またカルボキシ基がアルコールと反応することでエステル化,アミンと反応することでアミド化されます.下に示しておきますね.
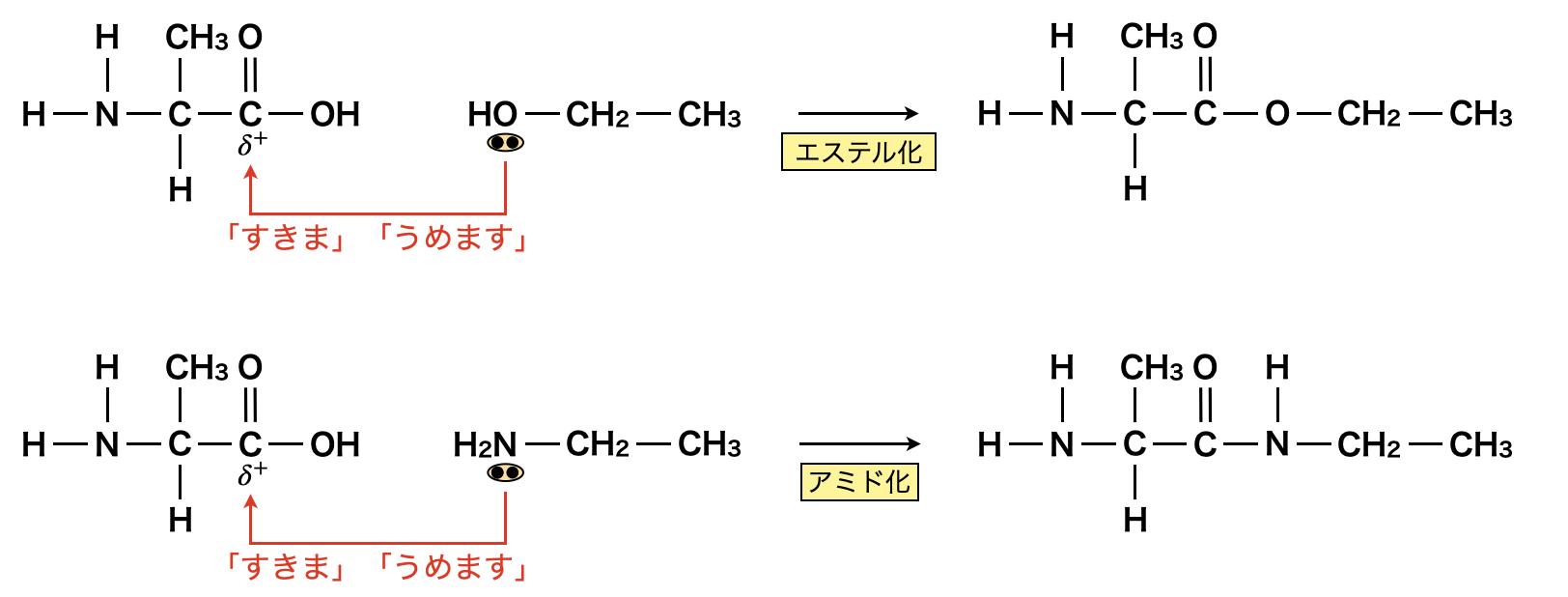
双性イオン
中性付近の\(\rm{pH}\)においては,カルボキシ基(\(\rm{-COOH}\))からアミノ基(\(\rm{-NH_2}\))へ\(\rm{H^+}\)イオンが移動し,\(1\)分子の中にカチオン(陽イオン)とアニオン(陰イオン)が共存するようになります.
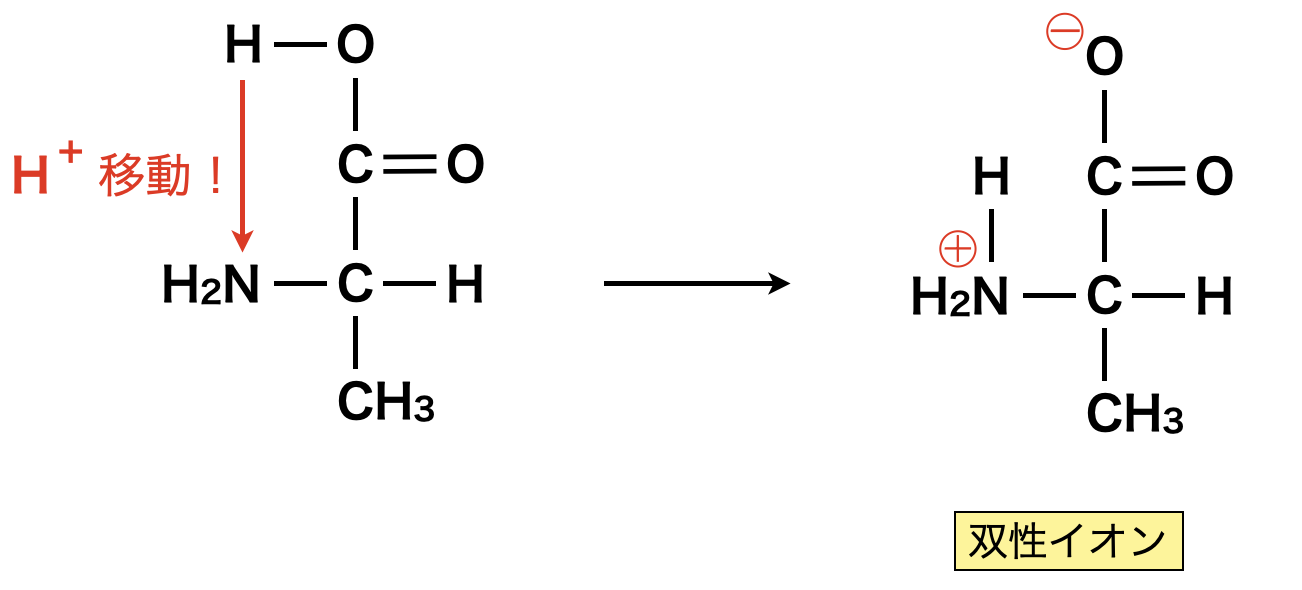
また\(\alpha-\)アミノ酸は結晶中でも双性イオンになり,分子間でイオン結合するため,\(\alpha-\)アミノ酸の融点は高くなります.
電離平衡
\(\alpha-\)アミノ酸は双性イオンが存在するため,電離平衡についてもしっかりと理解しておく必要があります.この理解が次に解説する等電点につながってきますよ!
中性アミノ酸の電離平衡
中性アミノ酸から考えていきましょう.
中性アミノ酸としてアラニン(Ala)を例として考えていきます.先ほども説明したように中性アミノ酸であるアラニンには,カルボアニオンとアミノカチオンが分子内に同時に存在する双性イオンが存在します.
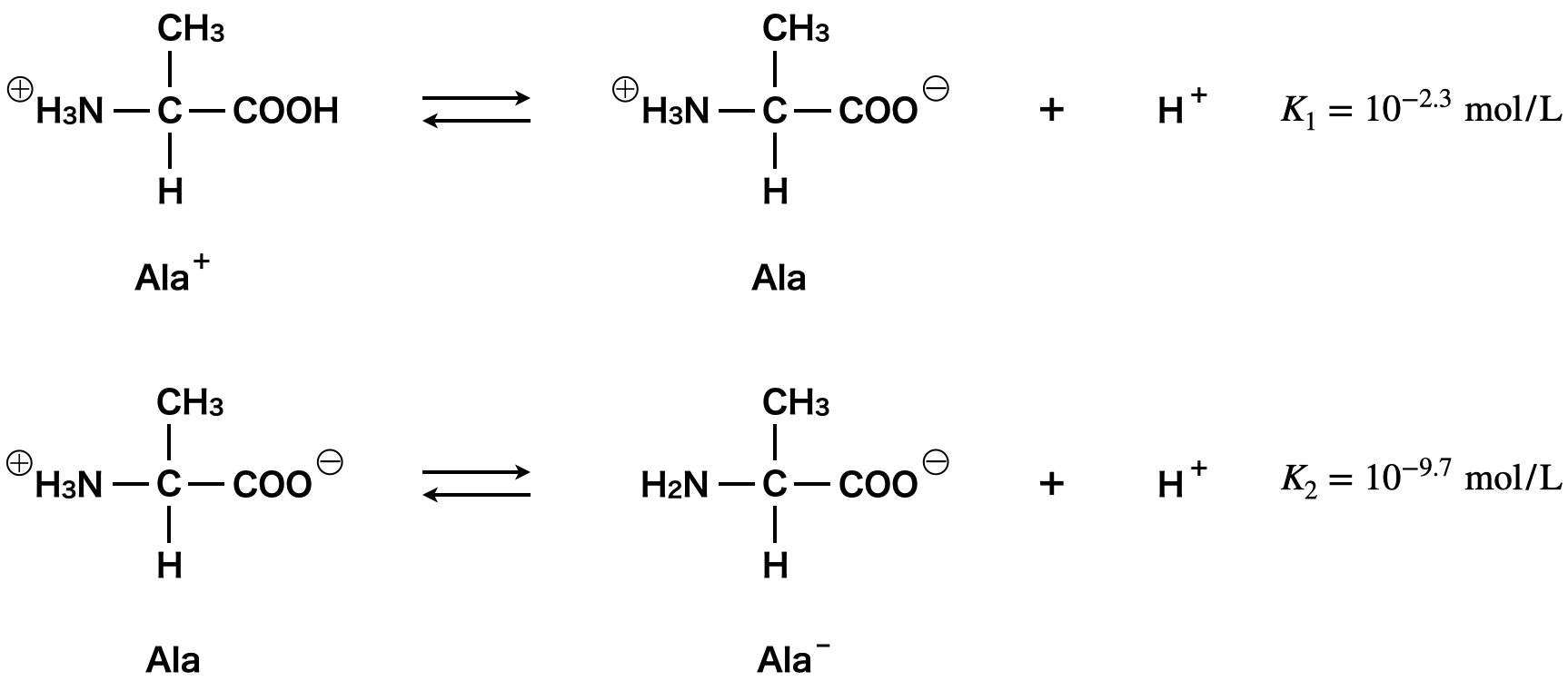
水溶液の液性が酸性(\(\rm{H^+}\)が多い)になると,ル・シャトリエの原理より左方向(\(\rm{H^+}\)が少なくなる方向)へ平衡が移動します.そのため,酸性溶液ではAla+が多くなります.
逆に塩基性(\(\rm{OH^-}\)が多い \(\rm{= H^+}\)が少ない)になると,ル・シャトリエの原理より右方向(\(\rm{H^+}\)が多くなる方向)へ平衡が移動します.そのため,塩基性溶液ではAla–が多くなります.
各\(\rm{pH}\)におけるAla+・Ala・Ala–の分布は下のようになります.
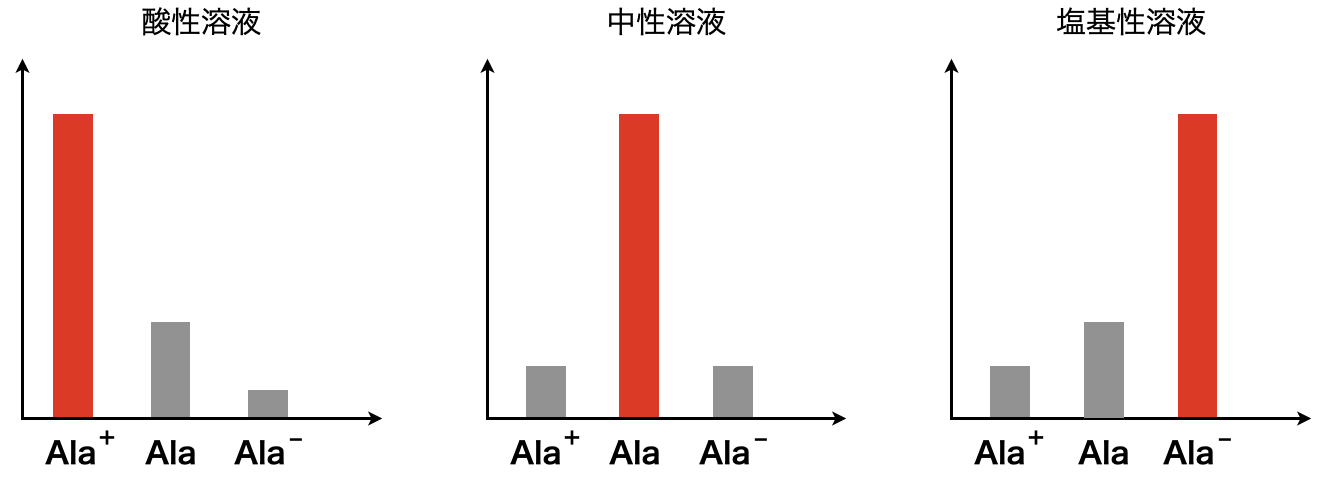
酸性アミノ酸の電離平衡
酸性アミノ酸の例としてグルタミン酸(Glu)で考えていきましょう.
中性アミノ酸との違いは,カルボキシ基が\(1\)つ増えているということです.そのため,酸性アミノ酸であるグルタミン酸の電離平衡は以下のようになります.
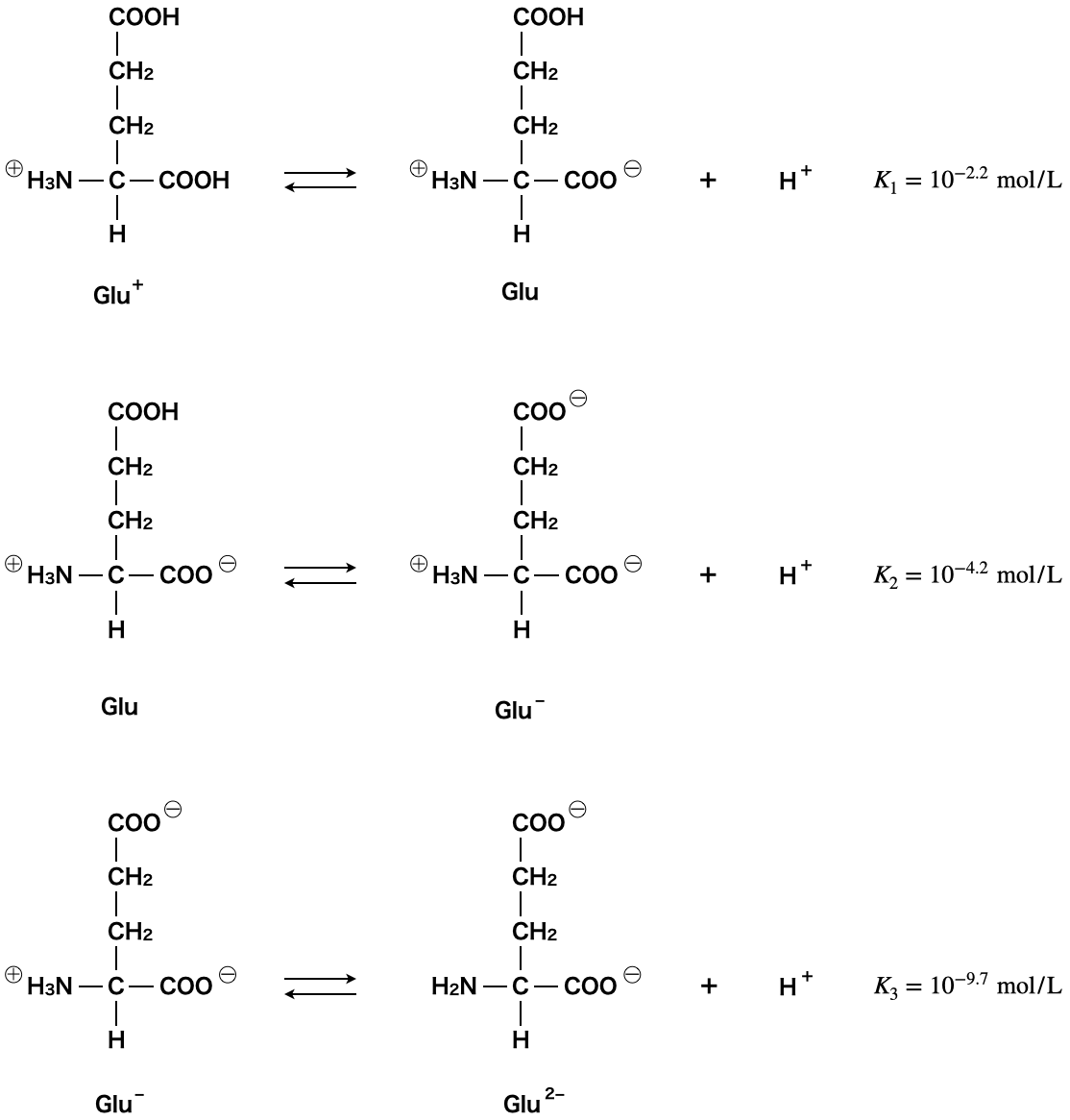
こちらも先ほどと同じように,酸性条件ではGlu+が多くなり,塩基性条件ではGlu2-が多くなります.中性条件のとき,どのような構造をとるかはしっかりと確認しておく必要があります.
側鎖のカルボキシ基(\(\rm{-COOH}\))は以下のように表され,その電離定数はおおよそ\(\rm{10^{-5}\ mol/L}\)となります.
\(\rm{K = \large \frac{[-COO^-][H^+]}{[-COOH]} \small = 10^{-5}\ mol/L}\)
中性付近では,\(\rm{[H^+] = 10^{-7}\ mol/L}\)なので,これを代入すると,
\(\rm{\large \frac{[-COO^-]}{[-COOH]} \small = \large \frac{100}{1}}\)
となり,側鎖のほとんどがカルボアニオン(\(\rm{-COO^-}\))となっていることがわかります.よって,中性条件ではGlu–となります.
各\(\rm{pH}\)におけるGlu+・Glu・Glu–・Glu2-の分布は下のようになります.
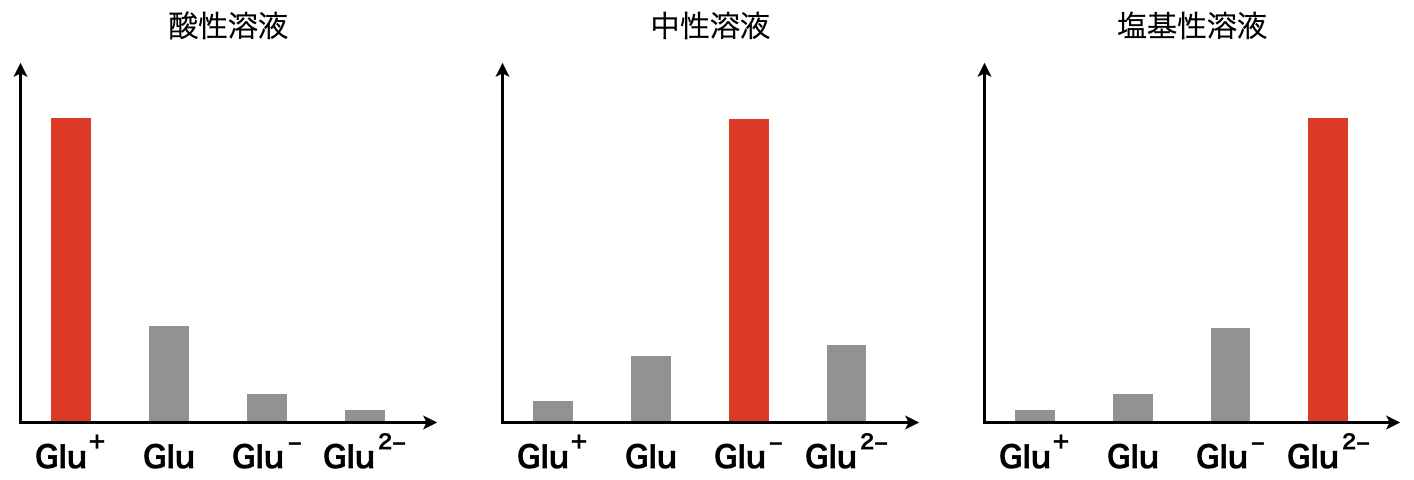
塩基性アミノ酸の電離平衡
塩基性のアミノ酸としてリシン(Lys)を考えていきましょう.
中性アミノ酸との違いは,アミノ基が\(1\)つ増えているということです.そのため,塩基性アミノ酸であるリシンの電離平衡は以下のようになります.

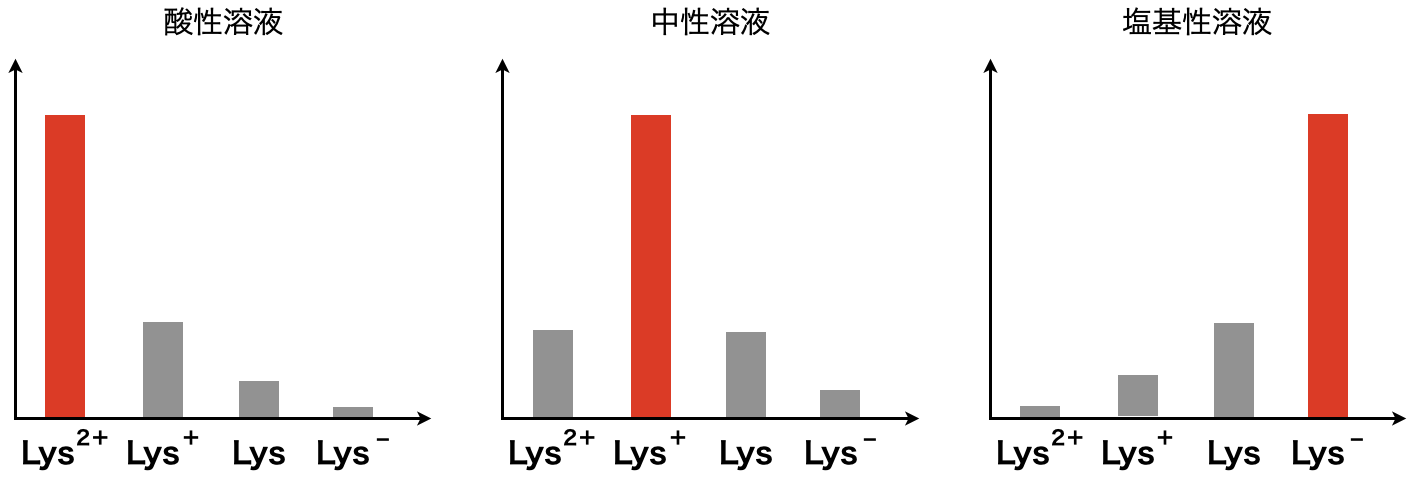
こちらも先ほどと同じように,酸性条件ではLys2+が多くなり,塩基性条件ではLys–が多くなります.そして中性条件では,Lys+が多くなります.
各\(\rm{pH}\)におけるLys2+・Lys+・Lys・Lys–の分布は下のようになります.




コメント