
大問\(4\)の総評
こんにちは,KUTです.
本記事では,\(2020\)年京大化学の大問\(4\)について解説していきます.
また解説に加えて,それぞれの問題で覚えておいてほしいポイントについて詳しく説明していきます.
京大の化学は難しいという印象が強い方が多いと思いますが,京大化学には難しい問題と標準問題の\(2\)つがあります.ここで,受験生が対策すべきことが\(2\)つあります.
\(1\)つ目は,標準問題を最後まで解き切る力を身につけることです.これにより,まずは平均点を取ることを目指します.
\(2\)つ目は,難しい問題と標準問題を見分けられる目を養うことです.試験本番は時間制限内に自分の解ける問題を解き切る必要があります.そのため,難しい問題は解かずに,標準問題をしっかりと選択していきながら,最後まで解いていくことが必要になります.
この記事では,問題を選択していく目を養うために,どのようにして判断していくのかということも自分なりに説明していきます.
それでは,\(2020\)年京大化学の大問\(4\)の解説に進んでいきましょう!
今回の高分子の問題は,フィッシャー投影図法から環構造を決定できるようになることが基本です.
ただその中で,\(\alpha\)型・\(\beta\)型を見極める必要があったり,受験生が初めて目にする「保護」という考え方を誘導によって導くような問題があります.このような問題は時間制限がある中では非常に難易度が高かったと思います.
このような問題は誘導でどこまで理解できるかが勝負になります!今回の解説でしっかりと理解していきましょう!
それでは今日も頑張っていきましょう!
大問\(4\)
問\(1\)
この問題は与えられた\(\rm{L}\)-ソルボースの鎖状構造から五員環構造を書く問題です.普段からフィッシャー投影図法を使って天然有機物を理解していることが重要になります.
鎖状構造から環構造を書くポイントは\(2\)つになります.
\(\rm{Step1:}\)結合する\(\rm{OH}\)基を回転させる
\(\rm{Step2:}\)「すきま」「うめます」で攻撃
\(\rm{Step1}\)
鎖状構造→環構造へ変化させるためには,その前に準備が必要です.その準備とは,結合する\(\rm{OH}\)基を回転させて結合させやすくする必要があります.
具体的に説明すると,今回の問題では\(5\)位の\(\rm{C}\)に結合した\(\rm{OH}\)基の\(\rm{O}\)原子がもつ非共有電子対が\(2\)位のカルボニル基へ「すきま」「うめます」の要領で攻撃します!
そこで\(5\)位の\(\rm{C}\)原子を回転させることで,\(\rm{OH}\)基を一番下にします.このように回転させることで,左側が上,右側が下となり,各原子団の上下を正確に捉えることができます!

\(\rm{Step2}\)
\(\rm{Step2}\)では実際に\(2\)位のカルボニル基へ「すきま」「うめます」の要領で攻撃します.この\(2\)ステップを踏むことで,下のような環構造が出来上がります!
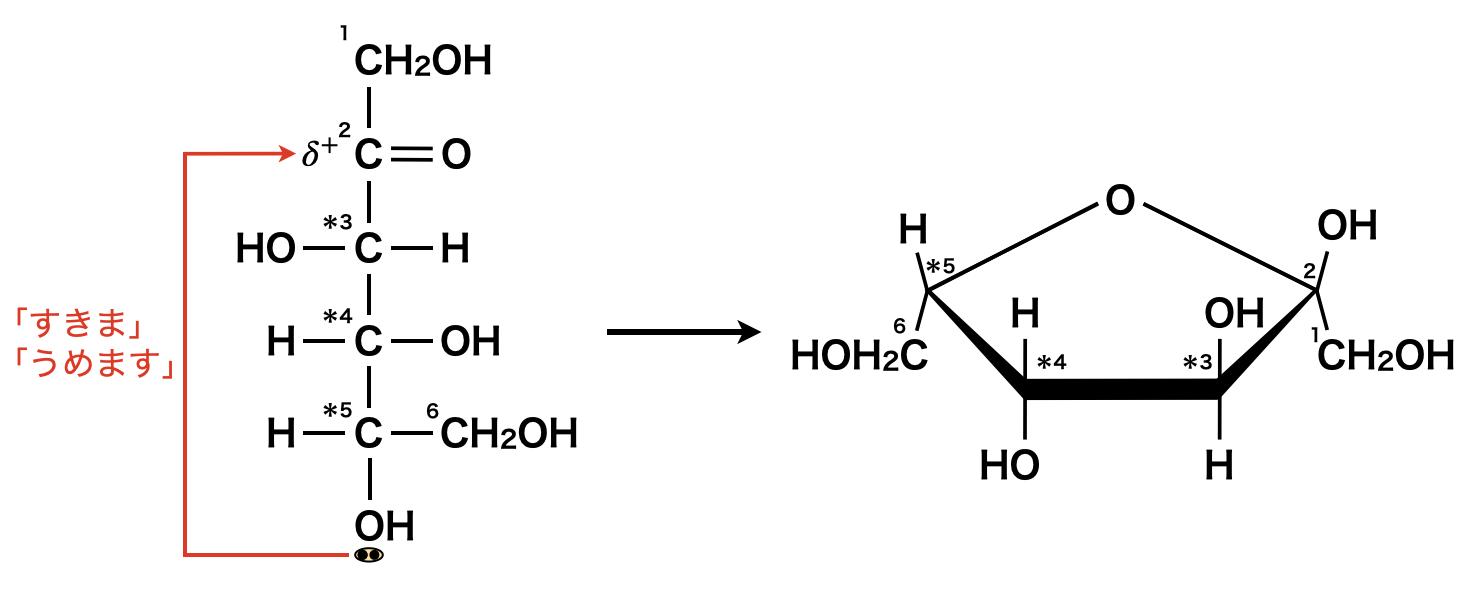
「すきま」「うめます」を知らないという方は私のこちらの記事をご覧ください!

問\(2\)
\((\rm{\hspace{.18em}i\hspace{.18em}})\)
「保護」についてはほとんどの方が初見だと思います.そのためこの問題には\(\rm{a}\)〜\(\rm{c}\)のような例による誘導があります.
このような問題は,誘導を上手く使えるかどうかが鍵となります.京大の入試問題では誘導付きの問題がたまに出てくるので,誘導にのれるようになっておきましょう!
まず,「アセタール化」について確認しておきましょう!アセタールは非常に重要なので,ここで丁寧に説明しておきます!アセタールのポイントは\(2\)つです!
\(\rm{Step1:}\)ヘミアセタールの形成
\(\rm{Step2:}\)ヘミアセタール→アセタール
\(\rm{Step1}\)
まずカルボニル基に\(\rm{OH}\)基が「すきま」「うめます」の要領で攻撃します!こちらは問\(1\)の考え方と同じですよ!これによってヘミアセタールを形成します.
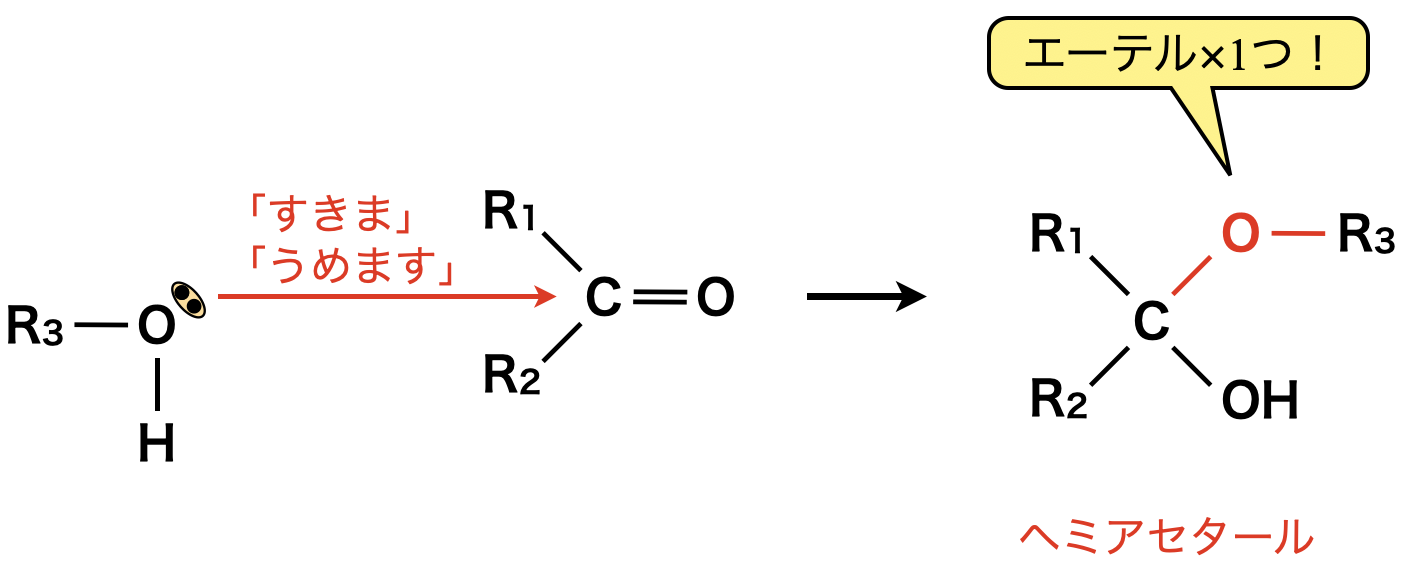
\(\rm{Step2}\)
次に,このヘミアセタール構造の\(\rm{OH}\)基は反応性が大きいため,\(\rm{R_4}\)-\(\rm{OH}\)のもつ\(\rm{OH}\)基とも縮合します.これにより生成する構造をアセタール構造といいます.
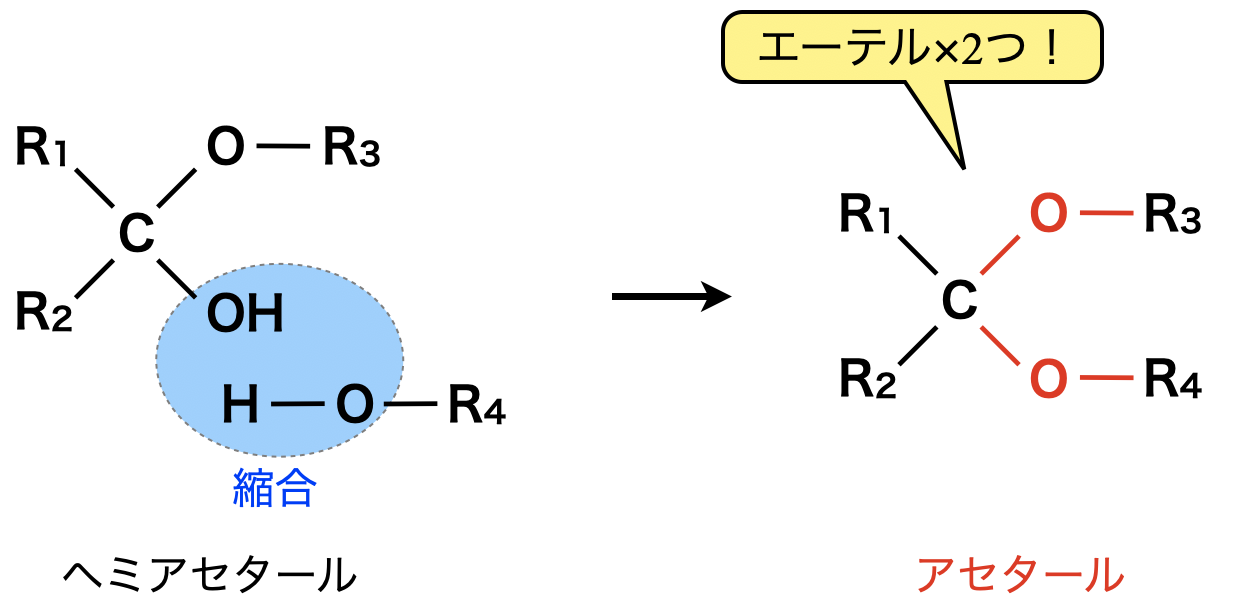
同じ\(\rm{C}\)原子にエーテル結合が\(2\)つ結合した構造をもつものをアセタール(\(\rm{acetal}\))といいます.つまり,ダブルエーテルということです!ここでのポイントは「同じ\(\rm{C}\)原子」に結合している必要があるということです.
一方,同じ\(\rm{C}\)原子にエーテル結合と\(\rm{OH}\)基をもつものをヘミアセタール(\(\rm{hemiacetal}\))といいます.ヘミアセタールは\(\rm{hemi=half}\),つまりアセタールと比較して半分のエーテルしかないよ!ということです!
英語で物質名を考えることで,少し覚えるのが楽になりますね!
それでは次に,この問題の誘導にある\(\rm{a}\)の物質を例として「保護」について考えていきましょう!説明が長くなるので,下の図を見ながら読み進めてくださいね!
まず\(\rm{Step1}\)として,アセトンを近づけることでカルボニル基に\(\rm{OH}\)基の\(\rm{O}\)原子のもつ非共有電子対が「すきま」「うめます」の要領で攻撃します.これによってヘミアセタール構造になります.
\(\rm{Step2}\)として,そこからさらに隣接する\(\rm{OH}\)基が縮合することで,アセタール構造が形成されます.ここまでは大丈夫ですか?
次に,この物質を酸化反応させると,\(5\)位にある\(\rm{OH}\)基のみ酸化されます.つまり,\(1\)位,\(2\)位の\(\rm{C}\)にもともとあった\(\rm{OH}\)基がアセタール化によって酸化反応の影響を受けていないことがわかります!これが「保護」という意味になります.
保護された部分の\(\rm{C}\)を見ると,\(2\)つの炭素間でつながっているため,これを\(1\),\(2\)-型環構造といいます.
最後に,酸性条件下で加水分解することで,\(1\)位,\(2\)位にあった\(\rm{OH}\)基の保護がなくなります.
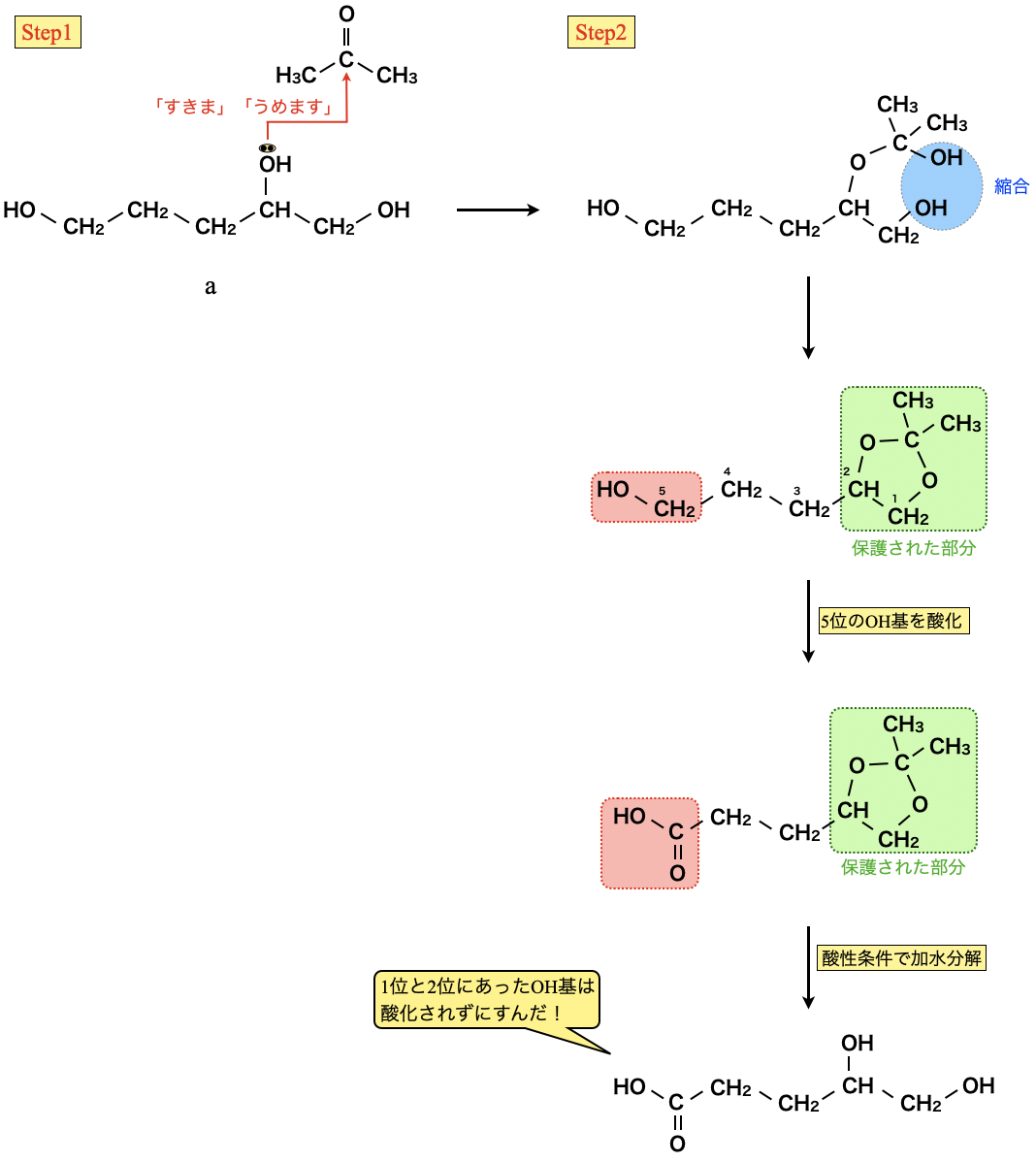
これが一連の「保護」した場合のアセタール化になります.
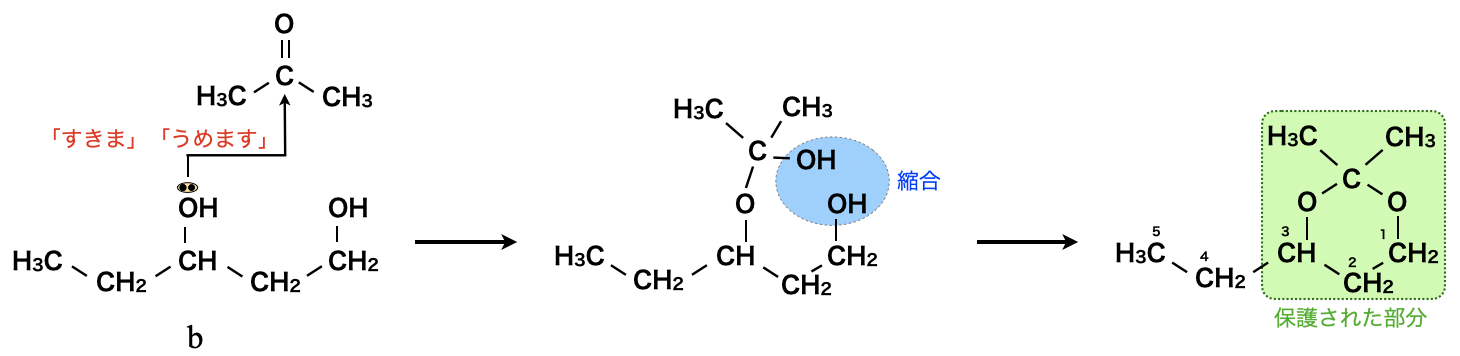
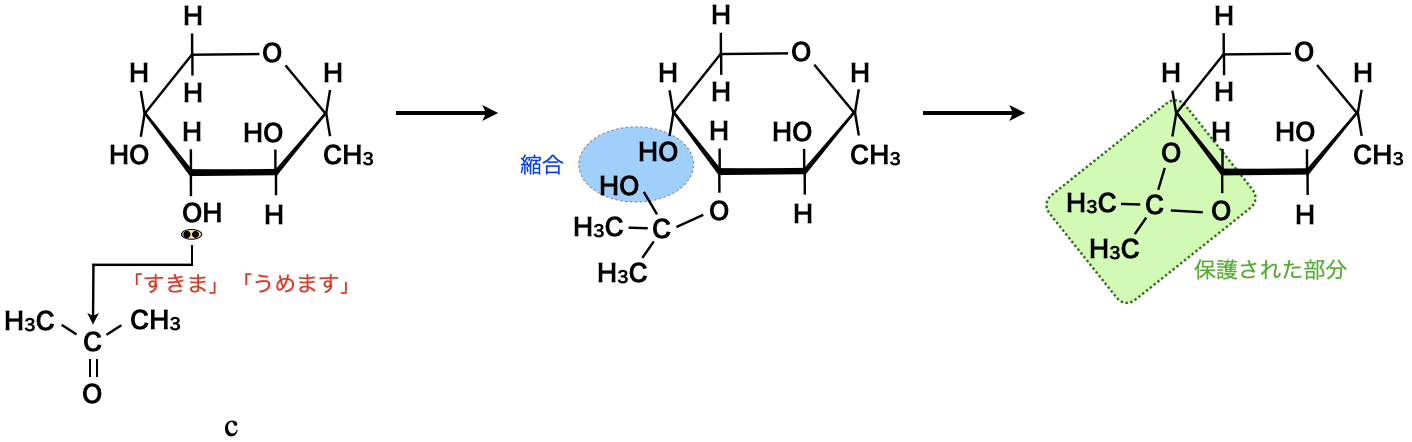
つづいて,\(\rm{b}\)や\(\rm{c}\)の場合も同じようにみていきましょう!
\(\rm{b}\)や\(\rm{c}\)については,保護までは同様に行います.ただしこの後については,それぞれ\(\rm{OH}\)基がなかったり,環構造であったりするため,酸化されることはありません.
さて,ここまでの誘導を理解することができましたか?それでは,やっとこさこの問題の\(\rm{L-}\)ソルボースについて考えていきます.
\(\rm{L}\)-ソルボースから\(\rm{2}\)-ケト-\(\rm{L}\)-グロン酸への酸化では,\(1\)位の\(\rm{CH_2OH}\)のみが酸化され,それ以外の\(\rm{OH}\)基や\(\rm{CH_2OH}\)基については保存されていることがわかります.そのため,次のような反応スキームを考えます!
問\(1\)の解答である五員環構造の\(\rm{L}\)-ソルボースがアセトンと反応することで,アセタール化されます.ここで,アセタール化するためには近接する必要があります.
そこで,\(2\)位と\(3\)位の上に向いている\(\rm{OH}\)基が\(1\),\(2\)-型環構造を形成し,\(4\)位と\(6\)位の下に向いている\(\rm{OH}\)基が\(1\),\(3\)-型環構造を形成します.
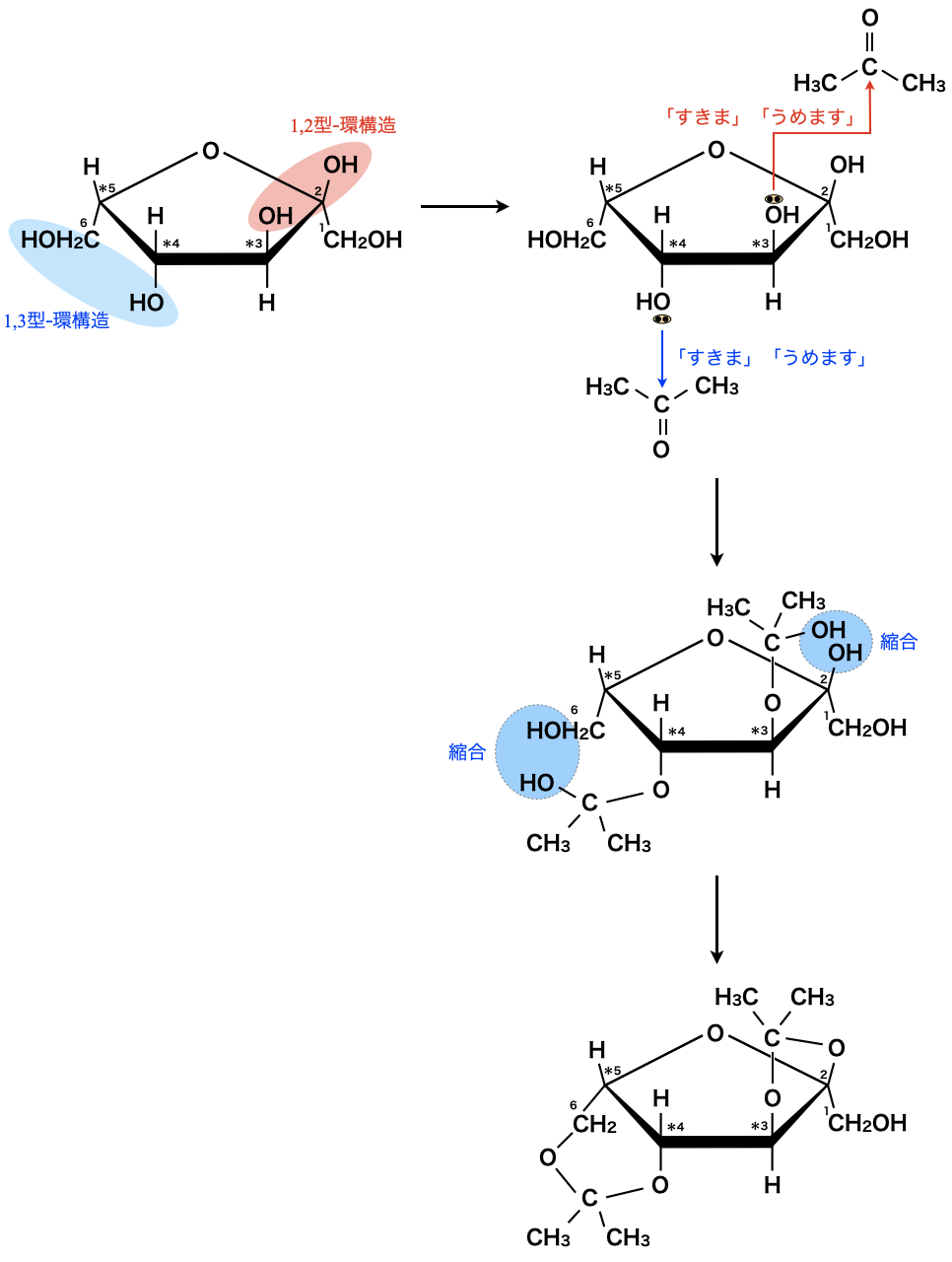
つまり,\(\rm{C2}\)および\(\rm{C3}\)に結合したものが\(1\),\(2\)-型環構造,\(\rm{C4}\)および\(\rm{C6}\)に結合したものが\(1\),\(3\)-型環構造となります.
\((\rm{i\hspace{-.01em}i})\)
五員環など環構造を自分で考える必要のある問題では,フィッシャー投影図法から環構造を導けるようになることが大切です.
問\(1\)とまったく同じ2ステップで環構造までもっていくことができます!
\(\rm{Step1}\)
五員環構造を作るためには,\(\rm{C4}\)を回転させ,\(\rm{OH}\)基を主鎖の一番下にします.
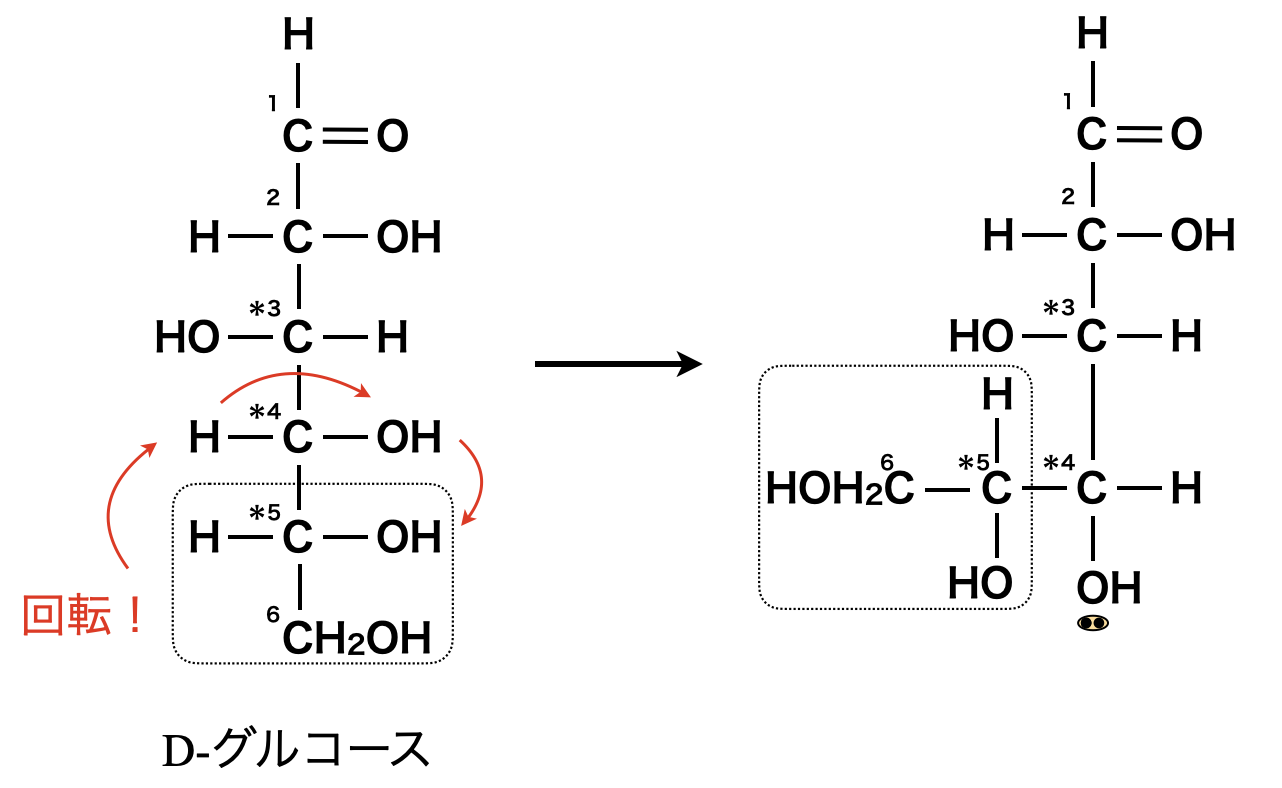
\(\rm{Step2}\)
そして\(\rm{C4}\)に結合する\(\rm{OH}\)基の\(\rm{O}\)のもつ非共有電子対が\(1\)位の\(\rm{CHO}\)に「すきま」「うめます」の要領で攻撃します.すると,下のような五員環構造のグルコースができます.
注意点としては,\(1\)位の\(\rm{OH}\)基が下であるのか?(\(\alpha\)型),上であるのか?(\(\beta\)型)はまだ決まっていないということです!

大切なのは,問題文に書かれている「\(2\)つの\(1\),\(2\)-型環構造が含まれる」という点です.
\(1\)つ目は,\(5\)位と\(6\)位が近い位置にあるので,ここで\(1\),\(2\)-型環構造をもつことができます.
\(2\)つ目については,水溶液中で存在する\(\alpha\)型と\(\beta\)型を考慮する必要があります.
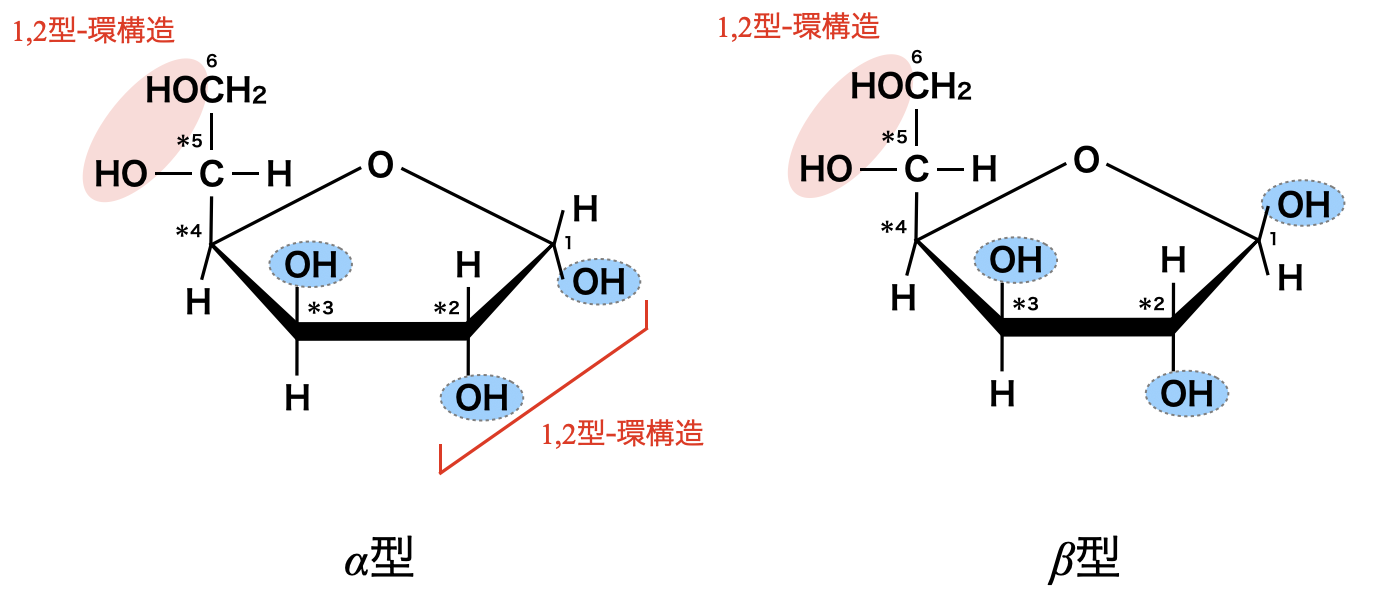
図を見ると,\(\alpha\)型では,\(\rm{OH}\)基の向きが\(1\)位と\(2\)位が下向き,\(3\)位が上向きとなっているので,\(1\)位と\(2\)位の\(\rm{OH}\)基の部分で\(1\),\(2\)-型環構造をもつことができます.
一方で,\(\beta\)型では,\(\rm{OH}\)基の向きが\(1\)位と\(3\)位が上向き,\(2\)位が下向きとなっているので,隣接した\(\rm{OH}\)基が存在しません.そのため\(\beta\)型では,\(1\),\(2\)-型環構造をもつことができません.

構造式を解答する際は,必ず記入例を見るようにしてください!
本問の場合は,構造式の記入例を見ると,立体構造がわかるように解答するべきだと判断できます.そのため,環以外の部分は立体構造がわかるように図示するように気をつけてください!
ただし,この問題で立体構造がわかるように解答するのは非常にレベルが高く,ほとんどの受験生がそこまではできていないと思います…(私個人的には,立体構造を明示できていなくても,部分点は最低あるのかな?と思ってますが…)
問3
いよいよ最後の問題です.
今回は\(2\)-ケト-\(\rm{L}\)-グロン酸→\(\rm{L}\)-アスコルビン酸の生成についての問題です.
\(\rm{L}\)-アスコルビン酸は\(5\)員環のため,\(1\)位にあるカルボン酸\(\rm{-COOH}\)基と\(4\)位の\(\rm{OH}\)基から脱水して縮合反応が起こり,環状エステルが生成していることがわかります.

エステル化では,\(\rm{COOH}\)基から\(\rm{OH}\)が,\(\rm{OH}\)基から\(\rm{H}\)が取れるため,取れた水分子に含まれる\(\rm{O}\)原子が縮合していた\(\rm{C}\)原子は\(\rm{C1}\)であることがわかります.
エステル化についてもこちらの記事で詳細に解説しています!

本問の補足として,ケト-エノール互変性についても解説しておきます.
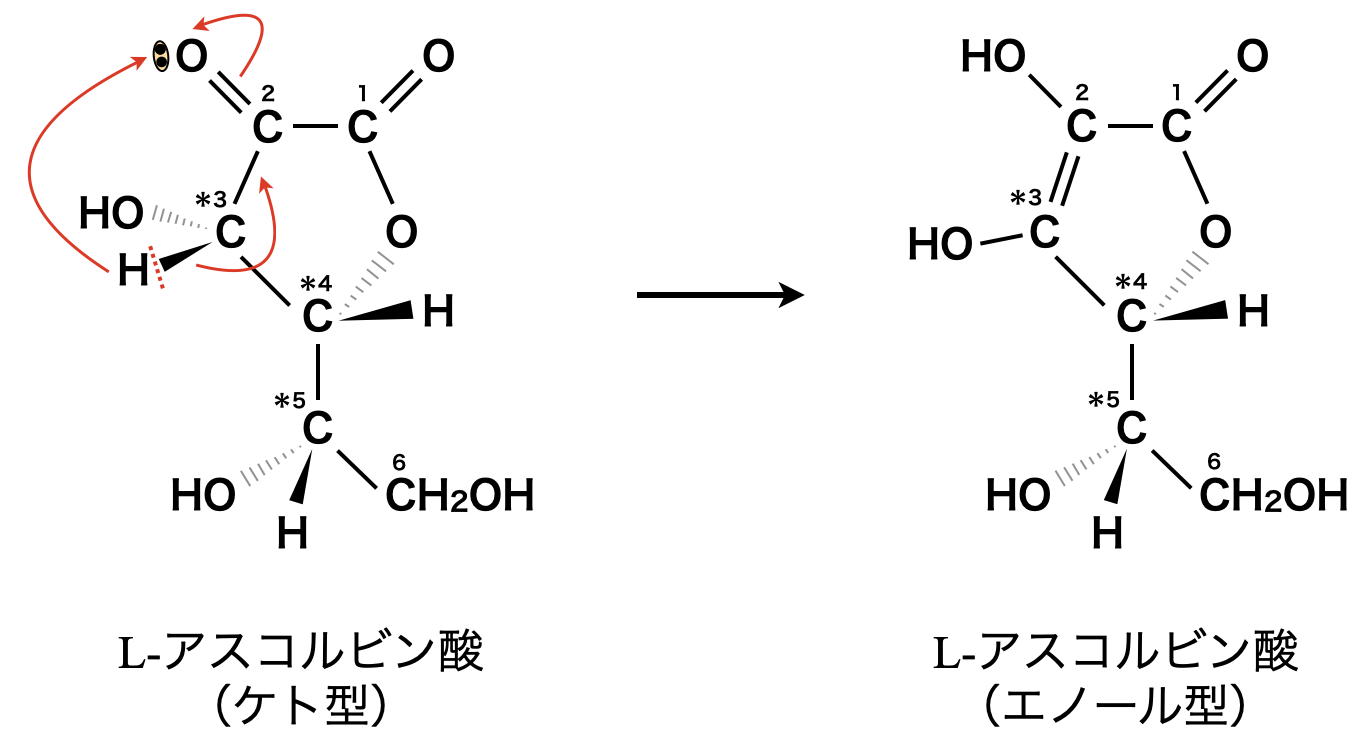
一般的には,エノール型よりもケト型の方が安定であると勉強したことがあるかもしれません.しかしながら,今回の問題ではケト型→エノール型となっています.これはおそらくエノール型の方がエネルギー的に有利(安定)であることが原因の1つであると考えられます.
ただこの事実を完全に理解する必要はなく,そのような例外がある!ということを知っておくことが大切です!このような例外を知っておき,それをテストで活用する場面が来たときには,今回でもあったように誘導がついているはずです!その誘導にしっかりとのれるようにしておきましょう!
最後に,ケト型→エノール型の電子の移動を記しておきますね!
最後に
最後まで閲覧していただきありがとうございました.
今回の問題は鎖状構→環構造にもっていくためにフィッシャー投影法でどのように考えるかがテーマでした.
フィッシャー投影法を使いこなすことができれば,未知の物質が出てきたとしても問題文の誘導にのることで,解くことができる問題も多くありますので,しっかりと解けるようになっておきましょう!
本記事の内容についてわからない点があれば,遠慮なく質問していただければと思います.
(Twitter:chem_story1)
京都大学の化学は難問が多いと言われますが,その分多くのことを学ぶことができます.
わからない問題に出くわしたときは,理解することでさらにレベルアップできる!というモチベーションで挑みましょう!
それでは皆さんの学習の一助になれば幸いです.



コメント