
有機化学の考え方
有機化学反応を学習していくと,ニトロ化やエステル化など様々な反応が出てきて,覚えにくいと思います.
これを暗記してなんとか乗り切ろうと思っていませんか?
各反応のプロセスを理解すると,その反応プロセスはたったの\(3\)通りに分類されます.
有機化学を結合の切断→再生という視点で捉えていきましょう!
結合の切断
\(\rm{A-B}\)という物質があったとします.この\(\rm{A,B}\)という物質の間には\(2\)つの電子を共有している共有結合があります.結合を切断するときに,それぞれの電子がどちらの原子につくかで,下の\(3\)通りの切断方法があります.
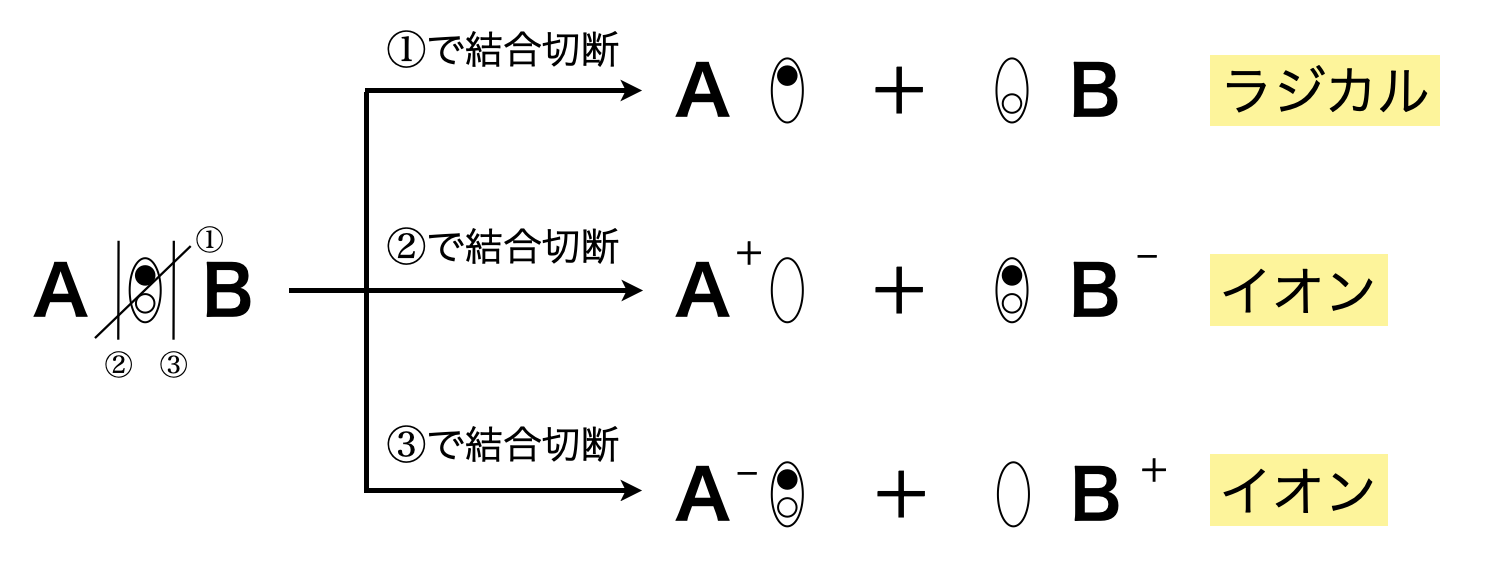
①では,電気的中性な原子,原子団であるラジカル(\(\rm{radical}\))が生成します.②や③では,陽イオンであるカチオン(\(\rm{cation}\))や陰イオンであるアニオン(\(\rm{anion}\))が生成します.
結合の再生
結合の再生には,先程説明したラジカル・陽イオン・陰イオンが別の共有結合に攻撃することで,新たな結合が生まれます.
①ラジカル反応
ラジカルが攻撃することで反応が起こります.

②求電子反応
陽イオンが攻撃することで反応が起こります.
名前がとっつきにくいですが,「陽イオンが負電荷をもつ電子を求めて反応しようとする」と覚えてください!

③求核反応
陰イオンが攻撃することで反応が起こります.
「陰イオンが正電荷をもつ原子核を求めて反応しようとする」と覚えてください!

まず,この前提をしっかりと覚えてくださいね!
結合の切断の判定
次は,結合を切断するときに,どのような状態がより安定しているのかを考えていきましょう!
結合している状態は非常に安定した状態となっています..そこから結合を切断することで,不安定な状態となります.そのため,先程説明した①〜③のいずれの反応が起こるかは,各物質の周りの環境によります.
例を考えてみましょう.
\(\rm{A-B}\)という物質があるとします.電気陰性度が\(\rm{A < B}\)の方が大きければ,\(\rm{B}\)が電子を引っ張る力が強いため,ラジカル反応か\(\rm{B}\)が陰イオン・\(\rm{A}\)が陽イオンとなる反応のどちらかが起こると考えられます.
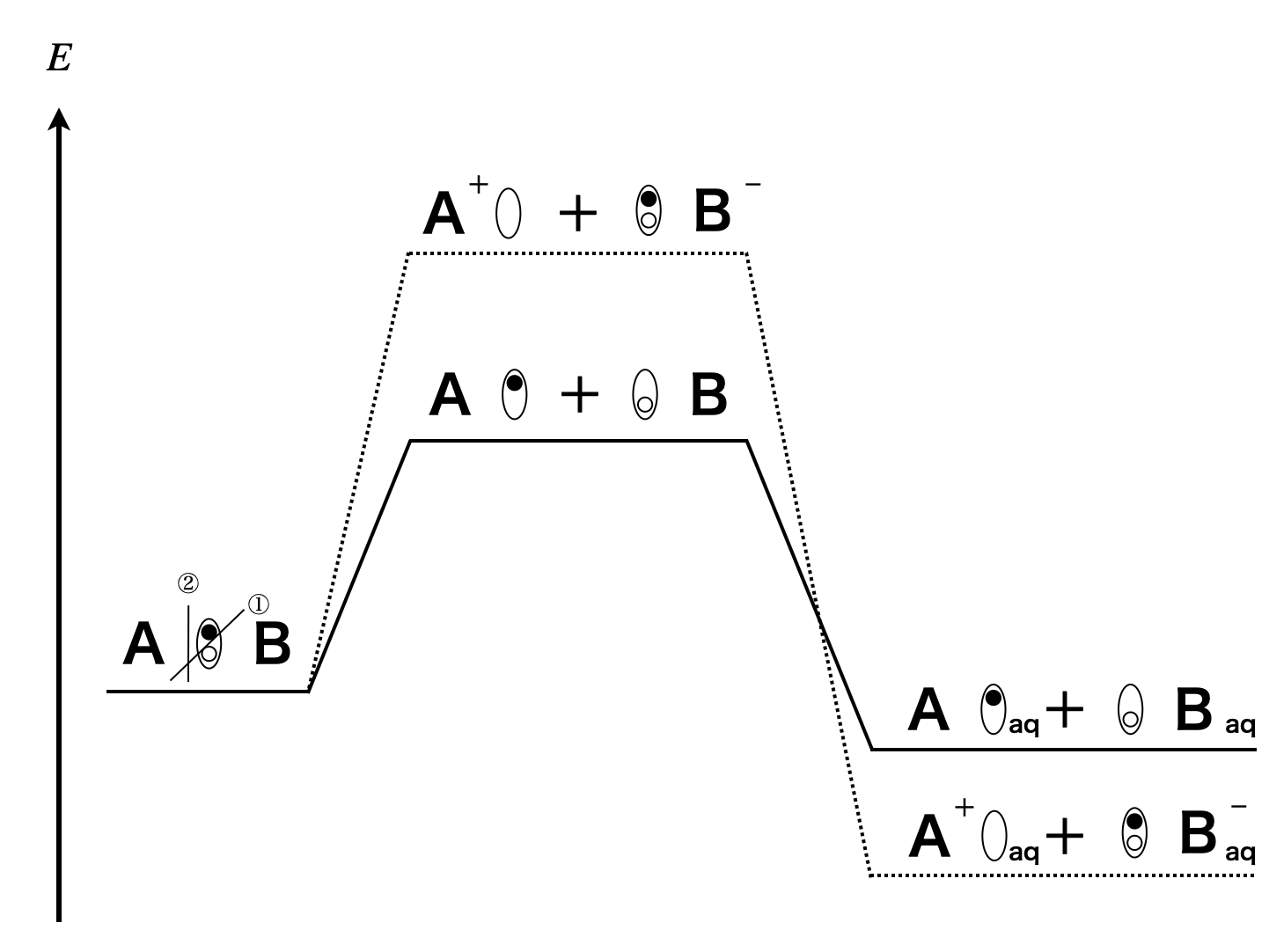
ここで,結合の切断に必要なエネルギーは,
ラジカル生成に必要なエネルギー < イオン生成に必要なエネルギー
となります!
そのため気相中・無極性溶媒中では,ラジカルが生じ攻撃する反応が起こりやすくなります.
また水のような極性溶媒中では,イオンが生成するような反応が起こりやすくなります.これはイオンが水和により安定することができるためです.
以上の\(3\)点をしっかりと覚えた上で,各反応を見ていきましょう!
この前提を理解しているかどうかで,この後の理解度が格段に変わってきます!!
アルカン
まずは,炭化水素について勉強していきます.
炭化水素とは,名前の通り構成元素が\(\rm{C}\)と\(\rm{H}\)のみからなる有機物のことをいいます.
アルカンってどんな物質?
まずはアルカンという名前について考えてみましょう.
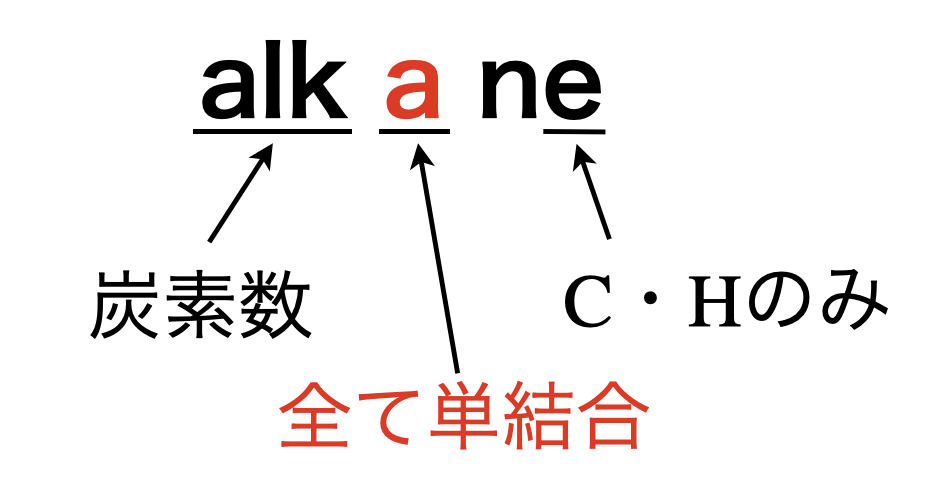
アルカンは構成元素が\(\rm{C}\)と\(\rm{H}\)のみからなり,全て単結合となっています.\(\rm{alkane}\)の「\(\rm{alk}\)」は炭素数を,「\(\rm{a}\)」は全て単結合,「\(\rm{e}\)」は構成元素が\(\rm{C \cdot H}\)のみであることを表しています.
そして直鎖状のアルカンは,分子量が大きくなるとファンデルワールス力が大きくなり,沸点も高くなります.
アルカンは
\(\rm{C1}\)〜\(\rm{C4}\):気体
\(\rm{C5}\)〜\(\rm{C16}\):液体
\(\rm{C17}\)〜:固体
と炭素数によって状態が変化することをおさえてくださいね!
アルカンの反応
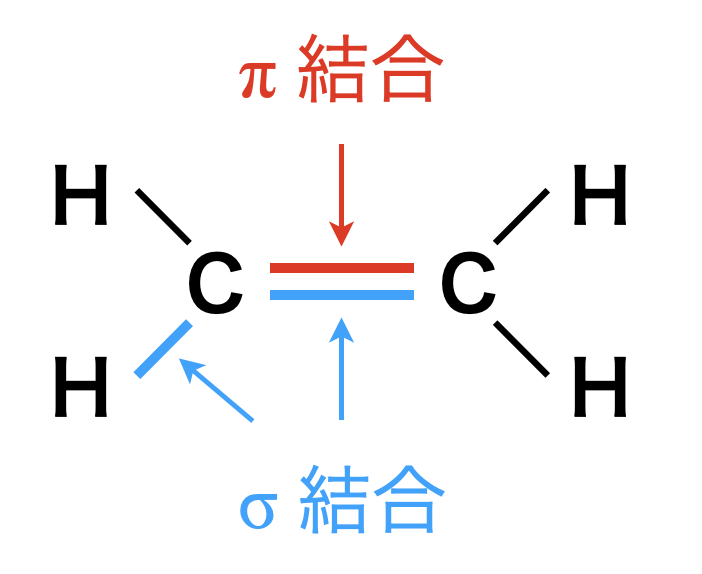
\(\rm{C-C}\)や\(\rm{C-H}\)の間の単結合を\(σ\)結合といいます.一方で,\(\rm{C=C}\)の間の結合の\(2\)番目を\(π\)結合といいます.
この\(2\)つの結合について比較すると,反応性としては\(π\)結合 \(> σ\)結合となります.アルカンは\(σ\)結合からなり\(π\)結合が存在しないため,反応性が乏しいです.
以下の\(2\)つの反応を理解しておけば大丈夫です!
\(\rm{Cl}\)ラジカルによる置換反応
\(\rm{Cl_2}\)は光を当てることで,\(\rm{Cl}\)ラジカルとなり反応が開始します.そして\(\rm{Cl}\)ラジカルがメタン中の\(σ\)結合からなる\(\rm{C-H}\)結合に攻撃することで,\(\rm{H}\)ラジカルを追い出します.に追い出された\(\rm{H}\)ラジカルは残った\(\rm{Cl}\)ラジカルと結合して\(\rm{HCl}\)となります.
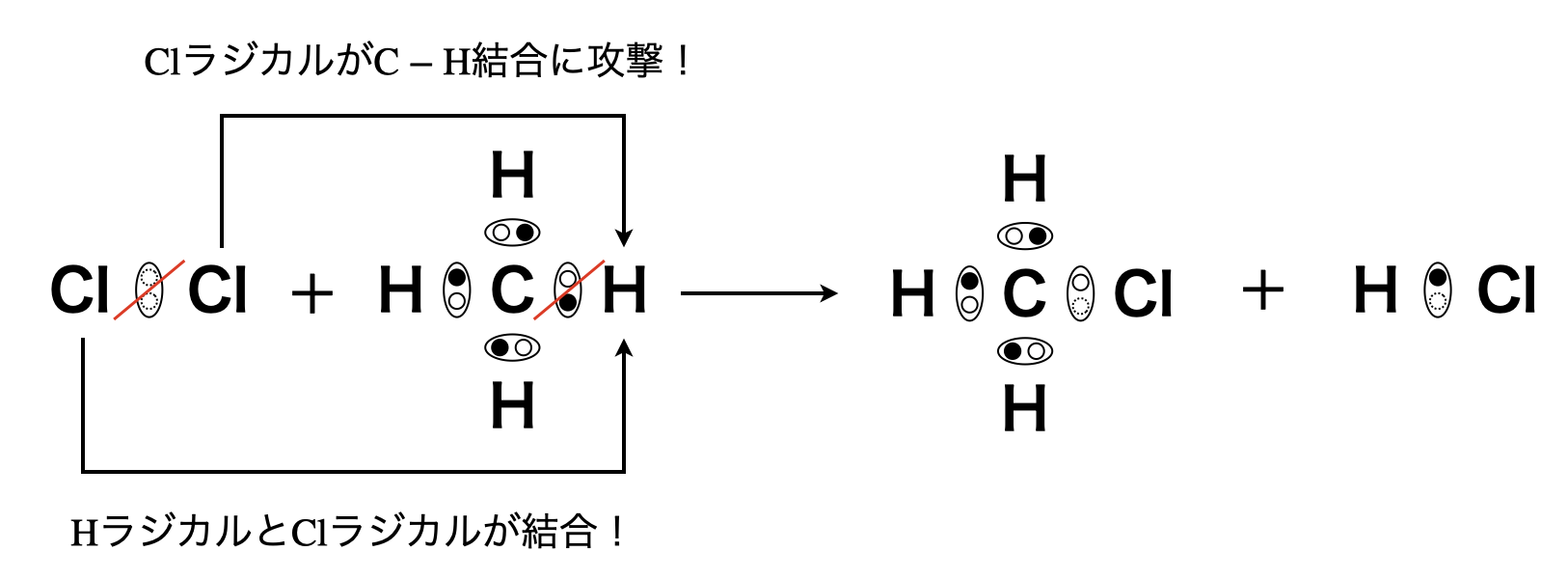
このように電子の動きから理解していくことで,暗記量を減らすことができますよ!
メタンに\(\rm{Cl}\)ラジカルが反応し続けることで,下のような置換反応が起こります.
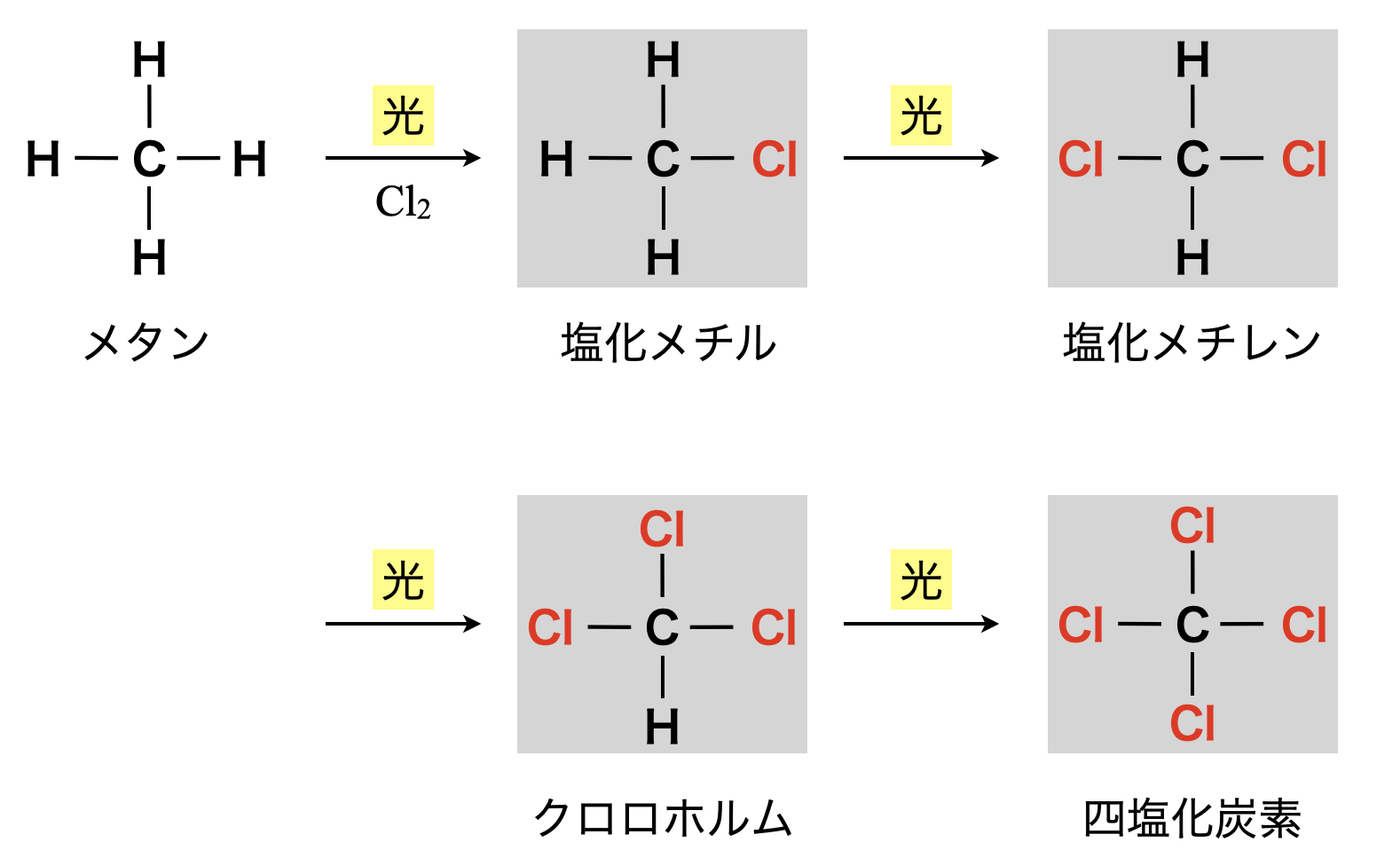
上の置換反応を繰り返し,メタン→塩化メチル→塩化メチレン→クロロホルム→四塩化炭素となります.
原油(ナフサ)の熱分解反応
原油は直鎖のアルカンが主成分となっています.その\(σ\)結合からなる\(\rm{C-C}\)が加熱により切断されることで,エチレンやプロペンなどが生成されます.
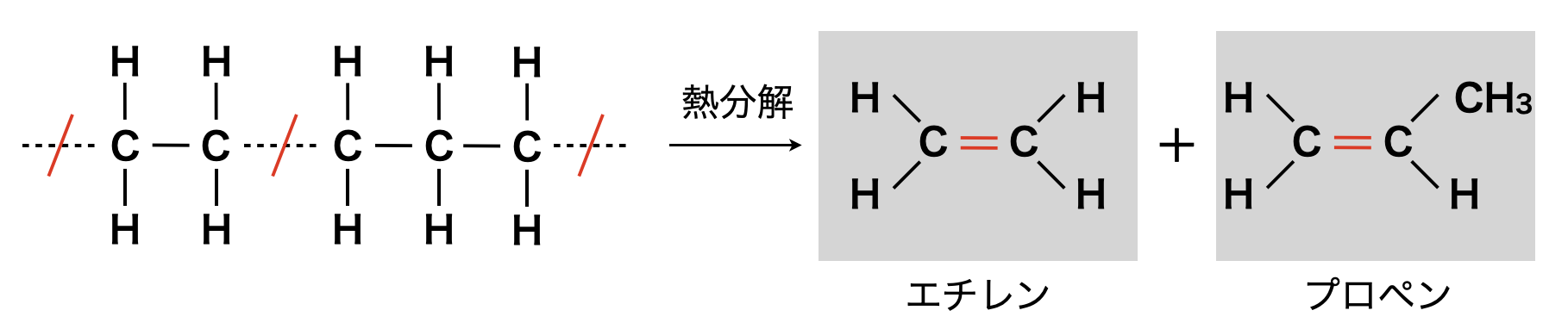



コメント